2021年 12月 内容改訂
登録義務者・唯一の代理人
1. 登録義務者
REACH発効1年後の2008年6月1日以降は、1企業当たり年間1t以上の物質それ自身または混合物中の物質をEU域内で製造または輸入する場合には、登録が義務付けられました。登録義務があるのはEU域内の製造者または輸入者ですが、EU域外の製造者には、輸入者に替えて、指名した唯一の代理人が登録する制度を設けています(EU域外の製造者は直接登録できません)。
2. 唯一の代理人
REACH規則による登録は、EU域外の企業はできませんので、輸入者がその義務を負うことになっています。一般的に、輸入者はREACH規則が要求する登録時の情報や評価時の対応に関する情報に乏しいと思われます。このため、EU域外の製造者は、「唯一の代理人」と契約し、登録に限らずREACH規則の義務などの代理をさせることができます。
唯一の代理人を活用することによりREACH規則への対応が円滑にできることや企業の生産情報などに関する情報の漏えいを防ぐことが可能になります。唯一の代理人はREACH規則の義務を遵守するため、物質の取り扱いに関する十分な背景(経歴)と物質に関する情報をもつことなどが必要です。そのほか、SDS(安全データシート)の最新版を常に提供することや登録物質の輸入量およびEU域内の顧客リストを常に最新の状態にする必要があります。
唯一の代理人はEU域内の自然人および法人であれば誰でもなれますが、登録などの実務を行えるのは、化学物質の知識と実務経験のあるEU域内のコンサルタント会社や各種試験機関などに限られてきます。これらのコンサルタント会社や各種試験機関は唯一の代理人業務のほかに、コンサルティングや化学物質の検査などのREACH規則に関するワンストップサービスを提供していますので、REACH規則に関する業務のすべてを任せることができます。
3. サプライチェーンにおける登録者の決定
EU域内輸入者はもとより、日本の原料メーカーおよび混合物メーカーも唯一の代理人を指定することで登録を行うことができるわけですが、EU域内輸入者までのサプライチェーンのいずれかの企業が登録すれば、その川下企業は登録が不要になります。塗料のような混合物を日本からEUに輸出するケースとして、日本の原料メーカー、日本の混合物メーカー、EU域内輸入者のサプライチェーンを例に考えると、サプライチェーンの川上に位置する原料メーカーが唯一の代理人を指名した登録すれば、その川下に位置する混合物メーカー、EU域内輸入者による登録は不要となります。
そのため、化学品の販売計画や製品等の秘密情報の有無、登録に伴う作業量、費用等を踏まえて、サプライチェーンの誰が登録するかを決定することになります。
段階的導入物質の登録の経緯
2008年6月1日からは、既存化学物質と新規化学物質の区別せずに、1企業当たり年間1t以上の物質は登録しなければ製造・輸入することができなくなりました。
しかし、欧州既存商業化学物質リスト(EINECS)に収載された物質などの段階的導入物質については、年間1t以上の場合、まず2008年6月1日~12月1日に予備登録をすることによって、登録期限に猶予を与えて順次登録が進められ、最終的には年間1t以上100t未満のトン数帯の2018年5月31日期限の登録を以って完了しました。
一方、非段階的導入物質や予備登録しない段階的導入物質については、年間1t以上製造・輸入する前に登録しなければなりません。
ここで段階的導入物質とは以下の3種類の物質です。
-
欧州既存商業化学物質リスト(EINECS:European Inventory of Existing Commercial Chemical Substances)に記載されている物質
-
欧州共同体または第4次、第5次もしくは第6次の欧州共同体加盟国において製造されたが、本規則発効前の15年間において少なくとも一度も製造者または輸入者により上市されたことがない物質(製造業者または輸入業者が文書による証拠をもっている場合に限る)。
-
欧州共同体または第4次、第5次もしくは第6次の欧州共同体加盟国において、1981年9月18日から1993年10月31日の間に製造者または輸入者によって上市された物質で、本規則の発効前に指令67/548/EECの第8条(1)の第1インデントに従って届出されたとみなされるが、本則に定められたポリマーの定義を満たさないもの、いわゆる「ノーロンガーポリマー(NLP)」(製造業者または輸入業者が文書による証拠をもっている場合に限る)。
上記以外の物質が非段階的導入物質です。
登録情報
REACH規則では、「一般的な登録」と「単離された中間体に対する登録」に分けて化学品庁に提出する情報が定められています。
1. 「一般的な登録」で要求される情報
一般的な登録のために提出が求められる情報には、次のものがあります。
(1)技術一式文書
(2)年間10t以上の場合は、化学物質安全性報告書(以降、CSRと言う)
(1)は年間1t以上の物質すべての登録に際して提出が求められる情報で、(2)は年間10t以上の物質に対して(1)に追加して求められる情報です。
技術一式文書に記載する情報は表1に示すとおりですが、登録者の身元情報、物質の名称などの識別情報、物質の製造および用途に関する情報、分類と表示、安全使用のための説明や物質の特性に関する情報などがあります。
CSRに記載する内容は、表2の通りです。物質の評価の結果、その物質が危険有害性を有する物質、PBT(難分解性・生物蓄積性・毒性のある物質)、あるいはvPvB(極めて難分解性で高い生物蓄積性がある物質)に該当する場合にはばく露評価とリスク評価を行います。このばく露評価とリスク評価を行う過程で、ばく露シナリオを作成します。ばく露シナリオは、川下企業にはSDSの付属書として提供されます。
ばく露シナリオは、どのように物質が製造され、そのライフサイクルを通して使用され、登録者がどのように人や環境に対するばく露を制御しているのかなどを取りまとめたものです。つまり、物質の放出、排出、漏洩などにより人の健康や環境に悪影響を及ばさないために、適切なリスク管理の情報を提供するものです。
技術一式文書(vi)項の情報は、登録トン数帯ごとに定められています。
「物理化学的特性」に関する情報はすべてのトン数帯で求められていますが、「毒性学的情報・人の健康に関する情報」や「生態毒性学的情報・環境に関する情報」はトン数帯が多くなるにつれ、求められる情報も多くなります。
例えば年間1~10tの場合は、以下の2条件(1)、(2)のうち少なくも一方に該当する場合は物理化学的特性に加え、毒性学的情報及び生態毒性学的情報が必要です。
一方、(1)、(2)のいずれにも該当しない場合は、物理化学的特性のみで登録ができます。
(1)CMRのカテゴリー1Aまたは1Bに該当、あるいはPBT・vPvBに該当することが見込まれる。
(2)下記aおよびbにともに該当する。
a. 特に分散的または拡散的用途で、消費者用の混合物に使用または成形品に組み込まれる。
b. CLP規則に基づき人の健康または環境に対し有害と分類されることが見込まれる。
2. 単離された中間体に対する登録
中間体はばく露や漏出が最小化されるよう強度に封じ込まれ、厳重に管理されたうえで使用または輸送されていることを条件に、その登録に要求される情報が軽減されています。つまり、物理化学的特性や人の健康または環境特性に関しては、追加試験が求められず、入手可能な既存情報の活用が認められています。そして、この使用や輸送の条件を満足しない場合には、前述の一般的な登録に必要となる情報の提出が必要となります。
中間体は、「サイトで単離された中間体」と「輸送を伴う単離された中間体」に分けて提出情報が定められていますが、登録者の身元情報や中間体の識別、分類、用途にかかわる情報など、求められる情報の大部分が共通しています。
なお、後者の「輸送を伴う単離された中間体」については、
(1)使用者が厳しく管理された状態で使用していることを登録者が確認すること
(2)1,000t以上の中間体については1~10tの登録で定められている物理化学的特性や毒性学的情報、生態毒性学的情報の提供
などが特に必要とされています。
表1 「一般的な登録」で提出が要求される情報
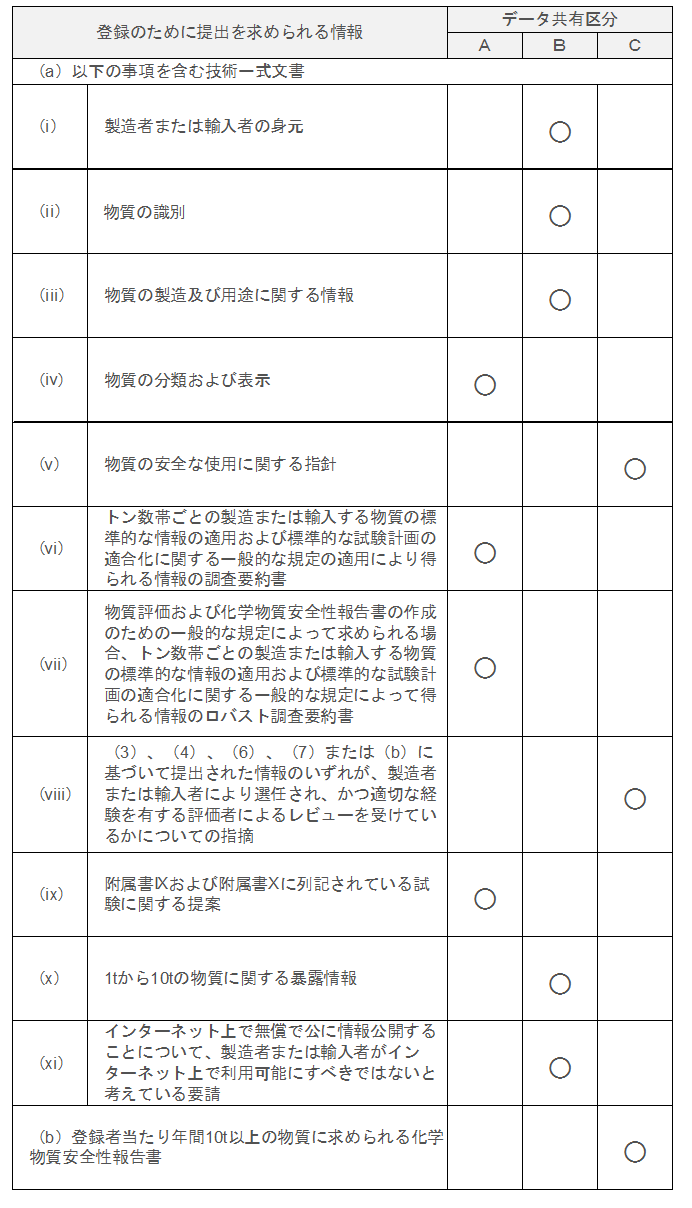
表2 化学物質安全性報告書(CSR)に記載する内容

登録に必要なデータの共有
1. 「1物質、1登録」の原則
REACH規則において、複数の登録者が同一の物質を登録する際、脊椎動物を使った試験などの調査の重複を防ぎ、試験データを共同で提出することにより企業が負担する費用を軽減することを目的とした、登録者間のデータ共有を促進する規定があります。
このようにREACH規則では登録される物質に関するデータを共有(「1物質1登録」という)するために、同一物質を登録済または登録しようとしている他社の有無を化学品庁に照会(Inquiry)しなければなりません。他社が存在しない場合は自社で必要なデータを全て準備しなければなりません。
一方、2021年8月末時点で、既に22,683物質が登録されていることから、少なくともこれらの物質については、登録済の他社が存在することになります。他社が存在する場合には、他社が登録済の各種データの共有、あるいは他社と分担した試験の実施等、登録に必要な情報を他社と協力して整備することになります。
なお、データ共有に関連して、オプトアウトという制度があります。これは以下の場合に、データの共有を行わず個別にテータ提出を行うことが認められるというものです。
(1)データ共有の費用負担が過大な場合
(2)データ共有が企業秘密に関わり、営業の損害をこうむる恐れがある場合
(3)リード登録者(データを共有している登録者の中から選ばれた物質を代表して登録する者)の提出した情報に合意できない場合
オプトアウトする場合、その理由を文書にして化学品庁に提出しなければなりません。
2. 共有しなければならないデータと個別に提出するデータ
物質の登録のために提出が求められるデータは、表1に示す、(A)登録者間で共有しなければならないデータ、(B)個別に提出するデータ、および(C)どちらかを選択できるデータに分類されています。
共有するデータは、最初に登録するリード登録者によって提出されます。
登録後の対応
登録を行えば、製造・輸入ができるわけですが、登録した情報の変更が生じた場合には、変更内容に応じた期間内(3カ月以内、6カ月以内、12カ月以内)に情報を更新しなければなりません。
また、化学品庁による登録文書のチェックや物質の評価等によって、追加的な情報の提供が求められる場合もあります。
当解説は筆者の知見、認識に基づいてのものであり、特定の会社、公式機関の見解等を代弁するものではありません。法規制解釈のための参考情報です。 法規制の内容は各国の公式文書で確認し、弁護士等の法律専門家に判断によるなど最終的な判断は読者の責任で行ってください。
情報提供:一般社団法人 東京環境経営研究所